药物动态 第15期

药品追溯码的问与答
2025年3月19日,国家医保局官网发布《国家医保局 人力资源社会保障部 国家卫生健康委 国家药监局关于加强药品追溯码在医疗保障和工伤保险领域采集应用的通知》,文件要求:医保定点医药机构要准确采集、核验药品追溯码并上传至全国统一的医保信息平台和药品上市许可持有人的药品追溯系统(中药饮片、中药配方颗粒、院内制剂、必须拆零发放的药品以及零散注射针剂等除外)。原则上,2025年7月1日起,销售环节按要求扫码后方可进行医保基金结算,对此前已采购的无追溯码药品,列入“无码库”管理,暂可进行医保结算。2026年1月1日起,所有医药机构都要实现药品追溯码全量采集上传。
一、药品追溯码是什么?流通过程中重复出现可能意味着什么?
答:药品追溯码是药品的“电子身份证”,通常由一系列数字、字母和(或)符号组成,标识在药品包装盒的显著位置,是每一盒药品从生产出厂时就被赋予的唯一身份标签。若在流通过程中药品追溯码重复出现,则该药品就可能是“回流药”、假药或是被串换销售。
二、如何通过追溯码发现“回流药”、药品被“串换”销售等线索,保护医保基金安全?
答:按照有关药品和医保管理规定,一盒药品卖给患者后,就不能再被卖给别的患者,只能卖一次,因此,一盒药品的追溯码,只应有一次被最终销售扫码的记录。若存在多次终端结算扫码记录,则该药品就可能是“回流药”或是被串换销售。一些不法分子使用医保基金购买药品后,不是自己使用,而是转手倒卖,将药品二次销售甚至多次销售,以骗取医保基金。这种经倒卖的药品被称为“回流药”。还有一些零售药店向参保人销售洗衣粉、化妆品等生活用品或非医保支付药品,并套用为医保药品进行结算,以达到非法套刷医保基金的目的,这种行为就是串换销售。这些违法行为,都会导致药品追溯码被重复扫码。在大数据的帮助下,医保部门就能根据药品追溯码提供的线索,对“回流药”、药品被“串换”销售等违法行为实现精准发现、精准打击,守好人民群众的“看病钱”“救命钱”。
三、什么时候能查询追溯码?
答:国家医保局正会同人社、卫健、药监等部门,共同研究制定文件,协同推进药品追溯码在医保、工伤领域的全流程、全量采集和全场景应用,努力在2025年6月底前实现应采尽采、应扫尽扫、能接尽接。可以预见的是,无追溯信息的医保药品和耗材将会越来越少,群众的用药安全将会得到有力保障。
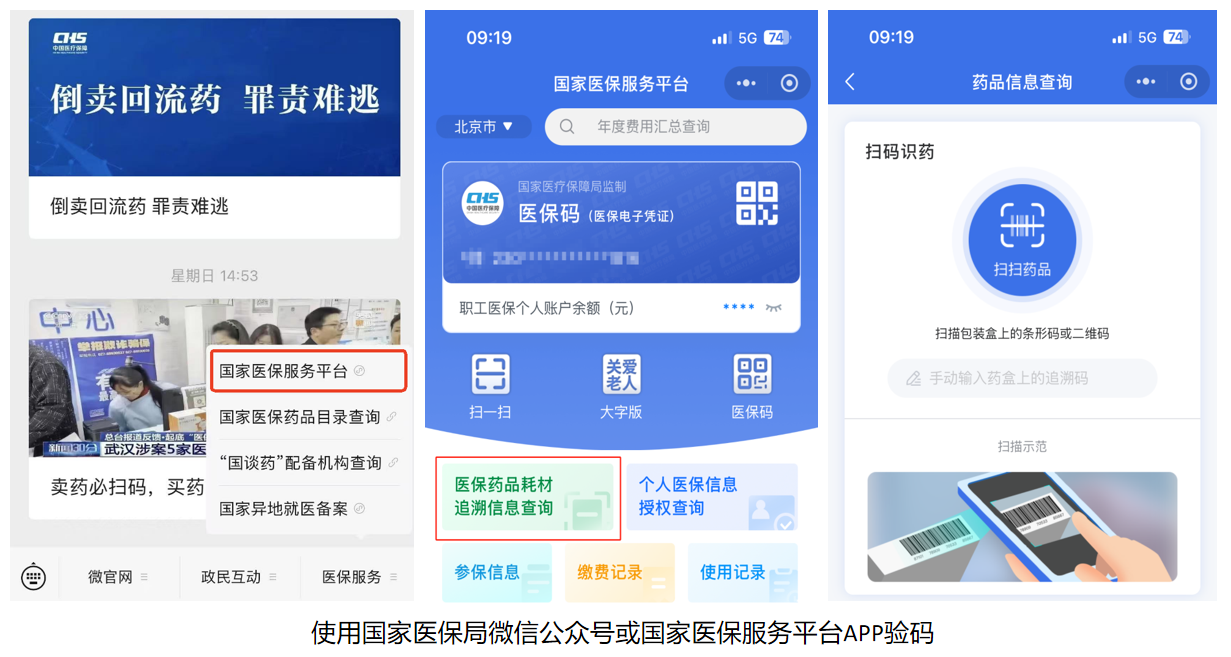
最后,广大医保参保人购药时请牢记五步法,用好药品追溯码,可以及时发现“回流药”等违法行为,维护自己的权益:
第一步,保留医院的结算单或者药店的购药发票。鉴于购药发票大多是热敏纸,字迹很容易消失,建议您在发票上的药名后,用黑色字迹中性笔标注上该药品的追溯码,然后手机拍照留存。第二步,药吃完后,把药盒上带有追溯码的部分连同药盒正面剪下来留存,避免保存整个药盒过于占地方。第三步,吃不完或者过期不能吃的药,一定不能整盒扔掉,不仅要把药盒剪角,而且要把内部成板的药物剪开,防止被不法分子捡到后转卖。如果您有时间,还可以把每一粒药剥离出来后再扔到指定的有害垃圾收集处。第四步,持续关注国家医保局微信公众号或当地医保APP。国家医保局已全面推动医保药品追溯码信息采集应用工作,后续将陆续发布有关医保药品重复追溯码的相关信息。第五步,一旦发现自己所购医保药品的追溯码与国家医保局发布的重复追溯码信息相同,或者医保APP上提示您药品追溯码有疑问,那表明该药有可能是“回流药”或者假药。建议您拿着剪下来的包含追溯码的部分药盒,连同留存的发票或发票照片,到购药的医院或者药店去沟通并获取解释,对确认的违法行为可以依法主张惩罚性赔偿。
(国家医疗保障局官网)

盐酸可乐定缓释片(商品名:力定儿)
【规格】 0.1mg*21片
【价格】 207.48元/盒 (国家医保谈判药品)
【厂家】力品药业(厦门)
【适应症】本品用于单独或辅助中枢兴奋药治疗6-17岁儿童和青少年的注意缺陷多动障碍(ADHD)。
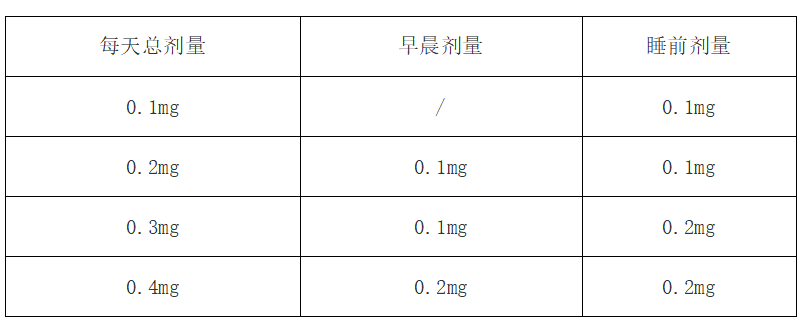
【用法用量】盐酸可乐定缓释片口服不受进食影响,服用时必须整片吞服,不得碾碎、咀嚼或者切割,否则会增加可乐定释放的速率。无论是单用或联合中枢兴奋药辅助治疗,给药剂量都应该根据治疗需要和患者耐受个体化调整剂量。起始剂量0.1mg,睡前单次服用;之后每隔1周剂量上调0.1mg/日,直至获得预期疗效。每日给药两次,两次剂量相同或睡前服用的剂量稍高。因临床试验中未评估,不推荐使用剂量高于0.4mg/日。
每天总剂量 早晨剂量 睡前剂量
【药理作用】可乐定可刺激大脑中的α2肾上腺素受体。可乐定不是中枢神经系统的兴奋剂。可乐定治疗注意力缺乏多动障碍(ADHD)的机理尚不清楚。另外,可乐定还是一种降压药,通过刺激脑干的α2肾上腺素受体,减少中枢神经系统交感神经冲动传出,降低外周阻力、肾血管阻力、心率和血压。
【药代动力学】吸收:盐酸可乐定缓释片的Cmax约为盐酸可乐定速释片的50%,Tmax比盐酸可乐定速释片迟5小时,在0.2到0.4mg/日的剂量范围,可乐定的血药浓度随着剂量的增加而增加;分布:分布至各器官,组织内药物浓度比血浆中高,能通过血脑屏障蓄积于脑组织;代谢:吸收剂量大约50%在肝脏代谢,消除半衰期与盐酸可乐定速释片类似,约为12-16小时,在6到17岁的年龄范围,可乐定的标准体重清除率随着年龄的增加略有下降,女性的标准体重清除率比男性低23%;排泄:虽然没有对盐酸可乐定缓释片进行肾功能损伤影响和可乐定排泄的研究,但其结果可能与速释制剂的结果类似(40%~60% 以原形于 24 小时内经肾排泄,20% 经肝肠循环由胆汁排泄)。
【不良反应】常见不良反应:嗜睡、疲劳、烦躁、失眠、噩梦、便秘、口干。严重不良反应包括低血压/心动过缓、镇静和嗜睡、反跳性高。导致停药最常见的不良反应为嗜睡和疲劳。
【注意事项】
①低血压/心动过缓:盐酸可乐定缓释片可导致剂量相关的血压和心率降低。在开始用药前、剂量增加后和用药期间应定期监测心率和血压。
②镇静和嗜睡:盐酸可乐定缓释片和其他中枢抑制剂(如吩噻嗪类、巴比妥类或者苯二氮卓类)合用前,要考虑潜在的附加镇静作用。应提醒患者在了解服用盐酸可乐定缓释片可能出现的反应前,不要操作重型设备和驾驶车辆。
③反跳性高血压:盐酸可乐定缓释片停药时,每日的总剂量应逐渐减少,每3到7天的递减量不能超过0.1mg,避免引起反跳性高血压。
④心脏传导异常: 可乐定的交感神经阻滞作用可能加重窦房结功能紊乱和房室阻滞,特别是对在服用其他交感神经阻滞药的患者。对有心脏传导异常的患者或合并使用其他交感神经阻滞药的患者,要缓慢增加盐酸可乐定缓释片的剂量并定期监测患者的生命体征。
⑤过敏反应:对可乐定经皮给药系统有局部接触过敏的病人,继续可乐定经皮给药或者口服盐酸可乐定替代治疗可能会引起全身皮疹。对可乐定有过敏反应病史的患者禁用,包括全身皮疹、荨麻疹、血管性水肿。
⑥由于缺少对照临床试验数据和不同的药代动力学特征,不推荐其他可乐定产品在同等的规格剂量下替代盐酸可乐定缓释片。
⑦可乐定过量:高血压可能提早发生,或可能伴随以下症状:低血压、心动过缓、呼吸抑制、体温过低、嗜睡、反应能力降低或缺乏、虚弱、易怒和瞳孔缩小。中枢神经系统抑制的频率儿童要高于成年人。大量过量用药可能导致可逆性心脏传导缺陷或者心律失常、窒息、昏迷和抽搐。药物过量的体征和症状一般在给药后30分钟到2小时内发生。
【特殊人群】
①老年人:本品不用于老年人。
②儿童:6岁以下儿童的安全性和有效性尚未明确。
③哺乳期妇女:孕妇用药发生出生缺陷和流产的风险未知,哺乳期妇女需慎用。
④肾功能损害患者:在儿童人群中尚未评估肾损伤对可乐定药代动力学的影响。盐酸可乐定缓释片的起始剂量应根据肾功能损伤程度而定。
【循证依据】
[1]中华医学会精神医学分会,中国医师协会精神科分会.中国成人注意缺陷多动障碍诊断和治疗专家共识[J]. 中华医学杂志, 2023,103(28): 2133-2144.可乐定缓释制剂作为非兴奋剂类α2- 肾上腺素能受体激动剂,对额叶皮质突触后膜α2受体具有激动作用,能够减轻ADHD症状、改善功能损害。推荐意见:药物治疗是成人ADHD的主要治疗手段,建议使用长效哌甲酯缓释制剂作为成人ADHD的一线药物治疗;当使用长效哌甲酯缓释制剂治疗成人ADHD效果不好或因不良反应不能耐受时,可使用托莫西汀作为二线药物治疗;上述药物效果不好或不能耐受时,推荐单用或联合使用可乐定或胍法辛作为三线用药。
[2]中华医学会儿科学分会发育行为学组,注意缺陷多动障碍早期识别、规范诊断和治疗的儿科专家共识[J].中华儿科杂志, 2020,58(03): 188-193.推荐哌甲酯类制剂为一线治疗药物。非中枢兴奋剂包括选择性去甲肾上腺素再摄取抑制剂和α2肾上腺素能受体激动剂两大类。选择性去甲肾上腺素再摄取抑制剂如盐酸托莫西汀,也为一线治疗药物。α2肾上腺素能受体激动剂包括可乐定、胍法辛等。
[3]药品说明书。

英国采取措施降低丙戊酸钠的生殖风险
2025年2月13日,英国人用药品和健康产品管理局(MHRA)网站发布了丙戊酸钠的安全性信息。
丙戊酸钠被批准用于治疗癫痫和双相情感障碍。已知母亲在怀孕期间服用丙戊酸钠可能会导致孩子出现严重的先天性畸形或神经发育障碍。与其他抗癫痫药物相比,使用丙戊酸钠的父亲所生的孩子患神经发育障碍的风险近期也已被报道。
研究表明,母亲怀孕期间使用丙戊酸钠与约九分之一的婴儿出生缺陷风险和约十分之三到十分之四的婴儿神经发育障碍风险有关。父亲在受孕前3个月使用丙戊酸钠,神经发育障碍的潜在风险要低得多,每100名婴儿中约有5名。丙戊酸钠对男性患者的其他生殖风险还包括人类不育症和在动物中发现的睾丸毒性证据。
2022年MHRA人用药品委员会(CHM)评估了丙戊酸钠生殖风险的最新数据,并在2022年12月发布的《药物安全更新》(Drug Safety Update)中提出建议措施。2023年11月28日的《国家患者安全警报》(National Patient Safety Alert)和2024年1月的《药物安全更新》为这些措施的实施提供了进一步的建议。这些新措施首先适用于所有55岁以下的新患者和已经接受专业人员评估的育龄女性。对于55岁以下开始服用丙戊酸钠的患者,须有两名专业人员评估的措施仍然有效,但CHM建议,目前正在服用丙戊酸钠的男性不需要进行评估。
CHM提醒医务人员:
对于首次开始服用丙戊酸钠的55岁以下患者:
●除非两名专业人员独立评估并证明没有其他有效或可耐受的治疗方法,或者有令人信服的理由表明不存在生殖风险,否则55岁以下的新患者(男性或女性)不得开始服用丙戊酸钠。对于许多患者来说,均有其他有效的方法可用于治疗双相情感障碍或癫痫。
●可以从临床指南(clinical guidance)中查找关于生殖风险可能不适用于患者的原因。
对于目前正在服用丙戊酸钠的育龄女性:
●在下一年度专业人员评估中,接受丙戊酸钠治疗的育龄女性应使用修订后的年度风险确认表对其治疗进行评估。在该次评估中,如果患者在开始或年度评估时从未接受过两名专业人员的审查,患者要继续服用丙戊酸钠时则需要第二名专业人员签字。育龄女性不需要被叫回来进行额外评估。一旦患者接受了两名专业人员的治疗评估,随后的年度评估只需要一名专业人员即可。
目前正在服用丙戊酸钠的男性:
●作为预防措施,建议男性患者及其女性伴侣在整个丙戊酸钠治疗期间和停止丙戊酸钠后的3个月内使用有效的避孕措施(避孕套加上女性伴侣使用的有效避孕措施),从而做到一个完整的精子周期内不接触丙戊酸钠。
●在下一次定期治疗评估中,与正在口服丙戊酸钠的男性患者讨论他们是否计划明年生孩子,如果是,则咨询一名专业人员确定最合适的治疗方案。
●建议男性在丙戊酸钠治疗期间和停止丙戊酸钠后3个月内不要捐献精子。
●如果女性报告自己怀孕或计划与使用丙戊酸钠的男性孕育子女,请她们进行产前咨询。
(MHRA网站)
澳大利亚警告男性服用丙戊酸钠所生孩子神经发育障碍的潜在风险
2025年3月7日澳大利亚治疗产品管理局(TGA)发布说明书修订信息,警告父亲暴露于丙戊酸钠可能引起的生育风险。
欧洲的一项回顾性观察性研究表明,与接受拉莫三嗪或左乙拉西坦治疗的男性所生孩子相比,在受孕前3个月内服用丙戊酸钠的男性所生孩子患神经发育障碍的风险可能更高。所研究的神经发育障碍包括孤独症谱系障碍、智力障碍、沟通障碍、注意力缺陷多动障碍和运动障碍。由于方法学的局限性,应谨慎解释本研究的结果。
作为预防措施,原研企业赛诺菲-安万特在产品说明书和消费者用药信息中增加了关于父亲暴露的新警告。TGA审查了企业提供的证据,并于2024年4月批准了在产品信息中添加警告的申请。丙戊酸钠仿制药企业也要求与原研药安全信息保持一致。
丙戊酸钠是一种已知的致畸原,在母体接触丙戊酸钠后,有先天性畸形(包括脊柱裂)和神经发育障碍的长期记录史。澳大利亚产品说明书已建议在怀孕期间避免使用该类药物,并对育龄女性使用这种药物提出建议。
英国最近对所有55岁以下的患者实行了丙戊酸钠的处方限制。为此,TGA进行了一项评估并就澳大利亚是否应效仿英国实施类似的限制性措施征求了药品咨询委员会的专家意见。委员会认为,自2018年评估该风险以来,母亲暴露后儿童的风险状况没有真正地变化,也没有足够的证据来修改丙戊酸钠的适应症或实施限制性措施来排除特定的患者群体。因此,TGA将继续常规监测这一安全信号。
澳大利亚TGA尚未收到与父亲接触丙戊酸钠有关的不良事件报告。
给医务人员的信息:
新的警告指导医务人员要告知男性患者服用丙戊酸钠的潜在风险,并讨论患者及其女性伴侣有效避孕的必要性。
应特别建议服用丙戊酸钠的男性患者:如果他们计划生育,在停止避孕之前,应咨询医生讨论替代治疗方案;如果女方怀孕并且在怀孕前3个月内他们服用过丙戊酸钠,应咨询医生;在丙戊酸钠治疗期间和停止治疗后3个月内不得捐献精子。
服用丙戊酸钠的男性应由在癫痫或双相情感障碍诊疗经验丰富的专家定期进行复查(至少每年一次),以评估含丙戊酸钠的药物是否仍然是最合适的选择,特别是在患者计划生育时。
产品信息中关于母亲暴露于丙戊酸钠的现有建议保持不变,TGA将继续进行常规安全性监测。鼓励育龄期并正在服用丙戊酸钠的患者与医务人员讨论相关风险。
(澳大利亚TGA网站)
